
Back Alleenpaar Afrikaans زوج غير رابط Arabic Parell solitari Catalan Volný elektronový pár Czech Lonepair Danish Freies Elektronenpaar German Μονήρες ζεύγος Greek Lone pair English Par solitario Spanish جفت الکترون غیرپیوندی Persian

U hemiji, usamljeni par ili slobodni elektronski par, odnosi se na par valentnih elektrona koji se ne dijele s drugim atomom u kovalentnoj vezi (IUPAC-ova definicija u Zlatnoj knjizi (Gold Book) [1] Ponekad se naziva i nepodijeljeni par ili nevezujući par. Usamljeni parovi nalaze se u najudaljenijem elektronskom omotaču atoma. Mogu se identificirati pomoću Lewisove strukture. Elektronski parovi se stoga smatraju usamljenim parovima ako su dva elektrona uparena, ali se ne koriste u hemijskoj vezi. Dakle, broj usamljenog parova elektrona plus broj vezujući elektroni jednak je ukupnom broju valencija elektrona oko atoma.
Koncept usamljenog para koji se koristi u teoriji odbijanja elektronskih parova valentne ljuske (VSEPR teorija) objašnjava oblike molekula. Oni su takođe navedeni u hemiji Lewisovih kiselina i baza. Međutim, hemičari ne smatraju sve nevezujuće parove elektrona usamljenim parovima. Primjeri su prijelazni metali kod kojih nevezujući parovi ne utječu na molekulsku geometriju i za koje se smatra da su stereohemijski neaktivni. U molekulnoj teoriji orbitala (potpuno delokalizirane kanonske orbitale ili lokalizirane u nekom obliku), koncept usamljenog para je manje različit, jer korespondencija između orbitale i komponenata Lewisove strukture često nije jednostavna. Ipak, zauzete nevežuće orbitale (ili orbitale uglavnom nevezujućeg karaktera) često se identificiraju kao usamljeni parovi.
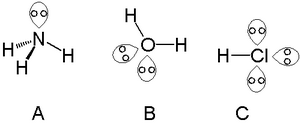
Jednostruki usamljeni par može se naći s atomima u dušičnoj grupi, kao što je dušik u amonijaka, a dva usamljena para mogu se naći s atomima u halkogenu. Skupina poput kisika u vodi i halogena može nositi tri usamljena para kao što je hlorovodik.
U VSEPR-teoriji elektronski parovi na atomu kisika u vodi čine vrhove tetraedra sa usamljenim parovima na dva od četiri vrha. H–O–H ugao veze je 104,5°, manje od 109° predviđenih za tetraedarski ugao, a to se može objasniti odbojnom interakcijom između usamljenih parova.[2][3][4] Predloženi su različiti računarski kriteriji za prisustvo usamljenih parova. Iako sama gustoća elektrona ρ (r) uglavnom ne pruža korisne smjernice u tom pogledu, otkriva se Lplaceova gustoća elektrona i jedan od kriterija za lokaciju usamljenog para je gdje je L (r) = – ∇2 ρ (r) lokalni maksimum. Minimum elektrostatskog potencijala V (r) je drugi predloženi kriterij. Još jedan uzima u obzir funkciju lokalizacije elektrona (ELF).[5]
- ^ lone (electron) pair
- ^ Organic Chemistry Marye Anne Fox, James K. Whitesell 2nd Edition 2001
- ^ Organic chemistry John McMurry 5th edition 2000
- ^ Concise Inorganic Chemistry J.D. Lee 4th Edition 1991
- ^ Kumar, Anmol; Gadre, Shridhar R.; Mohan, Neetha; Suresh, Cherumuttathu H. (6. 1. 2014). "Lone Pairs: An Electrostatic Viewpoint". The Journal of Physical Chemistry A (jezik: engleski). 118 (2): 526–532. Bibcode:2014JPCA..118..526K. doi:10.1021/jp4117003. ISSN 1089-5639. PMID 24372481.