
Back Natriumnitraat Afrikaans نترات الصوديوم Arabic Nitratu de sodiu AST سودیوم نیترات AZB Натриев нитрат Bulgarian Natrij-nitrat BS Nitrat de sodi Catalan Dusičnan sodný Czech Чили селитри CV Natriumnitrat Danish
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
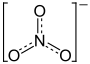
| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Natriumnitrat | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | NaNO3 | |||||||||||||||||||||
| Kurzbeschreibung |
farbloser, hygroskopischer Feststoff[3] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 84,99 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Dichte |
2,26 g·cm−3 (20 °C)[4] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Siedepunkt |
Zersetzung ab 380 °C[4] | |||||||||||||||||||||
| Löslichkeit |
leicht in Wasser (874 g·l−1 bei 20 °C)[4] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Natriumnitrat (auch Natronsalpeter oder Chilesalpeter), NaNO3, ist das Natriumsalz der Salpetersäure. Die chemische Verbindung liegt im reinen Zustand in Form einer hygroskopischen weißen Substanz oder farblosen Kristallen vor.
Natriumnitrat findet vielfältige Anwendung als Stickstoffdünger und in der Lebensmittelkonservierung sowie in geringerem Maße für die Herstellung von Glas oder Emaille. Ferner wird es auch für pyrotechnische Erzeugnisse oder Festtreibstoff für Raketenantriebe verwendet – allerdings nur eingeschränkt, denn obwohl Natriumnitrat in seiner Molekülstruktur dem auch heute noch häufig verwendeten Kaliumnitrat ähnelt, schränkt die hygroskopische Eigenschaft den Einsatz für die Pyrotechnik deutlich ein, primär der verminderten Lagerbarkeit und Stabilität wegen.
- ↑ Eintrag zu E 251: Sodium nitrate in der Europäischen Datenbank für Lebensmittelzusatzstoffe, abgerufen am 23. August 2020.
- ↑ Eintrag zu SODIUM NITRATE in der CosIng-Datenbank der EU-Kommission, abgerufen am 26. Februar 2020.
- ↑ Eintrag zu Natriumnitrat. In: Römpp Online. Georg Thieme Verlag, abgerufen am 27. November 2021.
- ↑ a b c d e f Eintrag zu Natriumnitrat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 3. Januar 2023. (JavaScript erforderlich)
- ↑ Datenblatt Natriumnitrat bei Merck, abgerufen am 19. Januar 2011.

