Back Natriumbikarbonaat Afrikaans بيكربونات الصوديوم Arabic Bicarbonatu de sodiu AST Natrium-hidrokarbonat Azerbaijani بیکربونات سودیوم AZB Натриев бикарбонат Bulgarian সোডিয়াম বাইকার্বনেট Bengali/Bangla Natrij-hidrogenkarbonat BS Hidrogencarbonat de sodi Catalan Hydrogenuhličitan sodný Czech
| Natria bikarbonato | ||
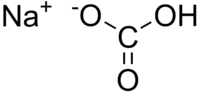
| Plata kemia strukturo de la Natria bikarbonato | ||
| Tridimensia kemia strukturo de la Natria bikarbonato | ||
| Alternativa(j) Nomo(j) | ||
| ||
| Kemia formulo | NaHCO3 | |
| PubChem-kodo | 516892 | |
| ChemSpider kodo | 8609 | |
| CAS-numero-kodo | ||
| Fizikaj proprecoj | ||
| Aspekto | blankaj senodoraj kristaloj | |
| Molmaso | 84.007 g mol−1 | |
| Smiles | [Na+].OC([O-])=O | |
| Denseco |
| |
| Refrakta indico | inter 1,3344 kaj
1,5000 | |
| Fandopunkto | 50 °C (122 ℉; 323 K) (malkomponiĝas al Natria karbonato | |
| Punto de malkomponiĝo |
270 °C (543.15 K) | |
| Acideco (pKa) |
| |
| Solvebleco en akvo |
||
| Solvebleco | ||
| Mortiga dozo (LD50) | 4220 mg/kg (buŝe, muso) | |
| Sekurecaj Indikoj | ||
| Risko | R38 R41 | |
| Sekureco | S22 S24/25 | |
| Pridanĝeraj indikoj | ||
| Danĝero
| ||
| GHS etikedigo de kemiaĵoj | ||
| GHS Damaĝo-piktogramo | ||
| GHS Signalvorto | Averto | |
| GHS Deklaroj pri damaĝoj | H320 | |
| GHS Deklaroj pri antaŭgardoj | P264, P305+351+338, P337+313 | |
Escepte kiam indikitaj, datumoj estas prezentataj laŭ iliaj normaj kondiĉoj pri temperaturo kaj premo (25 °C kaj 100 kPa)
| ||
La Natria bikarbonato aŭ Hidrogenkarbonato de natrio (laŭ IUTAK) estas kemia kombinaĵo kun molekula formulo NaHCO3, kristala blankokolora solido, solvebla en akvo, kaj gusto iomete alkala. Ĝi trovatas en naturo kiel la mineralo nakolito[1]. Ĝi same trovatas en la mineralo natro kaj troviĝas dissolvita en pluraj mineralfontoj. Ĝi enviciĝas en la nutroaldonaĵoj raportitaj de la Eŭropa Unio, identigita per E 500.
Pro tio ke ĝi estas konata ekde la antikveco, ĝiaj saloj estas vaste uzataj kaj por nutraĵo kaj por medicina traktado. En 1835, oni malkovris la kemian fermenton per miksaĵo da tartrata acido kun natria bikarbonato[2]. En 1850, oni anstataŭis la tartratan kremon je fosfata acido monokalcia kun sulfato de alumino kaj natrio, kaj la efekto pliboniĝis proksimume 60%.

- ↑ Lacustrine Sandstone Reservoirs and Hydrocarbon Systems: AAPG Memoir 95, Olive W. Baganz, Yuval Bartov, Kevin M. Bohacs, Dag Nummedal
- ↑ Foods & Nutrition Encyclopedia, Two Volume Set, Marion Eugene Ensminger, Audrey H. Ensminger