
Back Oksaalsuur Afrikaans حمض الأكساليك Arabic Oksalat turşusu Azerbaijani اقزالیک اسید AZB Шчаўевая кіслата Byelorussian Шчаўевая кісьля BE-X-OLD Оксалова киселина Bulgarian অক্সালিক অ্যাসিড Bengali/Bangla Àcid oxàlic Catalan Kyselina šťavelová Czech
| Okzalata acido | ||||||||
|---|---|---|---|---|---|---|---|---|
| ||||||||
| speco de kemiaĵo | ||||||||
| dikarboksilata acido • diprotic acid | ||||||||
| Ĝeneralaĵoj | ||||||||
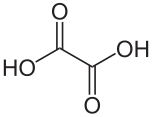
| Nomo | Okzalata acido | |||||||
| Kemia formulo | H2C2O4 | |||||||
| CAS-numero-kodo | 144-62-7 | |||||||
| PubChem-kodo | 971 | |||||||
| ChemSpider-kodo | ||||||||
| SMILES |
C(=O)(C(=O)O)O
| |||||||
| Karakterizaĵoj | ||||||||
| Molmaso |
90.03 g·mol−1 | |||||||
| Denseco |
1.90 g cm−3 (anhidra) | |||||||
| Fandopunkto | ||||||||
| Solvebleco | 143 g/L (25 °C) | |||||||
| Sekurecaj indikoj | ||||||||
| ||||||||
| Se eble, uziĝu unuoj de la Sistemo Internacia de Unuoj. Escepte de la notoj alie indikitaj, la datumoj rilatas al materialoj laŭ la ordinaraj normoj pri temperaturo kaj premo (25o kaj premo je 1 atmosfero aŭ 760 mm de Hg). | ||||||||
Okzalata acido[1] aŭ oksalata acido[2] estas organika kombinaĵo kies molekula formulo estas H2C2O4. Ĝi estas solida senkolora kristalo formante akvan senkoloran solvaĵon. Ĝi estas klasifikita kiel dukarboksilata acido. Rilate al acida forto ĝi estas pli forta ol la acetata acido. Okzalata acido estas reduktanta agento kaj ties konjuga bazo[3], konata kiel okzalata jono (C2O42−), estas kelata agento. Kutime, la okzalata acido nature troveblas en ties duhidratohava formo, H2C2O4.2 H2O. Troa konsumado de okzalata acido aŭ longedaŭra haŭtokontakto esteblas danĝera.




