
Back بوسبيرون Arabic بوسپیرون AZB Bwspiron Welsh Buspiron German Βουσπιρόνη Greek Buspirone English بوسپیرون Persian Buspironi Finnish Buspirone French בוספירון HE
| Buspirona | ||
|---|---|---|
 | ||
| Nombre (IUPAC) sistemático | ||
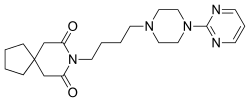
| 8-[4-(4-pyrimidin-2-ylpiperazin-1-yl)butyl]-8-azaspiro[4.5]decane-7,9-dione | ||
| Identificadores | ||
| Número CAS | 36505-84-7 | |
| Código ATC | N05BE01 | |
| PubChem | 2477 | |
| DrugBank | APRD00222 | |
| Datos químicos | ||
| Fórmula | C = 21 | |
| Peso mol. | 385.50314 g/mol | |
| Farmacocinética | ||
| Biodisponibilidad | 5% | |
| Unión proteica | 95% | |
| Metabolismo | Hepático | |
| Vida media | 2-3 horas | |
| Excreción | Orina (29-63%), heces (18-38%) | |
| Datos clínicos | ||
| Nombre comercial |
Ver lista Ansial®,
Ansiced® Buspar® | |
| Cat. embarazo | Los estudios en animales no han demostrado efectos adversos sobre el feto, pero no hay estudios clínicos adecuados y bien controlados hechos en embarazadas. Puede emplearse con vigilancia médica. (EUA) | |
| Estado legal | Solo receta | |
| Vías de adm. | Vía oral | |
Buspirona es una agente ansiolítico, no relacionado estructuralmente con las benzodiacepinas, barbitúricos u otros agentes ansiolíticos. Pertenece al grupo químico de las azapironas. Posee un extremo del tipo químico azaspirodecanodiona y pirimidinilpiperazina. Tiene un perfil distinto a las benzodiacepinas, fármacos comúnmente prescritos para tratar la ansiedad, al carecer de efectos hipnóticos, anticonvulsionantes, miorrelajantes, además de no alterar la memoria.[1] No produce dependencia, potencial de adicción ni efecto tolerancia.[2]
En 1986, Bristol-Myers Squibb obtuvo aprobación de la Administración de Alimentos y Medicamentos de Estados Unidos (en inglés Food and drug administration FDA) para la comercialización de la Buspirona. La droga se hizo genérica en 2001.
- ↑ J. Artigas-Pallarés (2004). «Nuevas opciones terapéuticas en el tratamiento del trastorno por déficit de atención/hiperactividad». Revista Neurol 38 (Supl 1): 117-123. Consultado el 19 de julio de 2015.
- ↑ Error en la cita: Etiqueta
<ref>no válida; no se ha definido el contenido de las referencias llamadasBarreto