
Back لايسين Arabic لیزین AZB Лизин Bulgarian লাইসিন Bengali/Bangla Lisina Catalan Lysin Czech Lysin German Λυσίνη Greek Lysine English Lizino Esperanto
| Lysine | |
 L ou S(+)-lysine 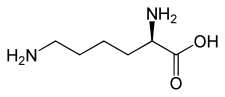 D ou R(–)-lysine |
|
| Identification | |
|---|---|
| Nom UICPA | Acide 2,6-diaminohexanoïque |
| Synonymes |
K, Lys |
| No CAS | (racémique) (L) ou S(+) (D) ou R(–) |
| No ECHA | 100.000.673 |
| No CE | 200-294-2 (L) 213-091-9 (D) |
| Code ATC | B05 |
| FEMA | 3847 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C6H14N2O2 [Isomères] |
| Masse molaire[1] | 146,187 6 ± 0,006 8 g/mol C 49,3 %, H 9,65 %, N 19,16 %, O 21,89 %, |
| pKa | 2,15 / 9,16 / 10,67 |
| Propriétés physiques | |
| T° fusion | 224,5 °C[2] |
| Solubilité | 642 g l−1 d'eau à 20 °C et 780 g l−1 d'eau à 30 °C |
| Thermochimie | |
| Cp | |
| Propriétés biochimiques | |
| Codons | AAA, AAG |
| pH isoélectrique | 9,74[4] |
| Acide aminé essentiel | oui |
| Occurrence chez les vertébrés | 7,2 %[5] |
| Cristallographie | |
| Paramètres de maille | L-lysine : a = 7,492 Å b = 13,320 Å |
| Propriétés optiques | |
| Pouvoir rotatoire | +14,6 |
| Précautions | |
| SIMDUT[7] | |
Produit non contrôlé |
|
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
La lysine (abréviations IUPAC-IUBMB : Lys et K) est un acide α-aminé dont l'énantiomère L est l'un des 22 acides aminés protéinogènes, et l'un des neuf acides aminés essentiels pour l'homme. Elle est codée sur les ARN messagers par les codons AAA et AAG[8]. Elle est caractérisée par la présence d'une fonction amine primaire à l'extrémité de sa chaîne latérale, ce qui en fait un résidu basique dans les protéines, tout comme l'arginine et l'histidine.
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ « Lysine ».
- ↑ (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams : Organic Compounds C8 to C28, vol. 2, Huston, Texas, Gulf Pub. Co., , 396 p. (ISBN 0-88415-858-6)
- ↑ (en) Francis A. Carey, « Table of pKa and pI values », sur Département de chimie de l'université de Calgary, (consulté le ).
- ↑ (en) M. Beals, L. Gross, S. Harrell, « Amino Acid Frequency », sur The Institute for Environmental Modeling (TIEM) à l'université du Tennessee (consulté le ).
- ↑ « Lysine », sur reciprocalnet.org (consulté le ).
- ↑ « Lysine (l-) » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ Donald Voet et Judith G. Voet, Biochimie, Bruxelles, Éditions De Boeck Université, , 2e éd. (ISBN 978-2-8041-4795-2), p. 1290


