
Back Distikstofmonoksied Afrikaans أكسيد النيتروس Arabic غاز مضحك ARZ Azot-1 oksid Azerbaijani دی نیتروژن مونوکسید AZB Диазотен оксид Bulgarian নাইট্রাস অক্সাইড Bengali/Bangla Dušik-suboksid BS Òxid de dinitrogen Catalan Oxid dusný Czech
| Protoxyde d'azote | |
 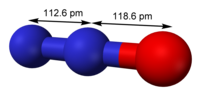 Structure du protoxyde d'azote. |
|
| Identification | |
|---|---|
| Nom UICPA | protoxyde d'azote |
| Synonymes |
oxyde nitreux |
| No CAS | |
| No ECHA | 100.030.017 |
| No CE | 233-032-0 |
| No RTECS | QX1350000 |
| Code ATC | N01 |
| PubChem | |
| ChEBI | 17045 |
| No E | E942 |
| FEMA | 2779 |
| SMILES | |
| InChI | |
| Apparence | gaz comprimé liquéfié incolore, d'odeur caractéristique[2]. |
| Propriétés chimiques | |
| Formule | N2O |
| Masse molaire[4] | 44,012 8 ± 0,000 7 g/mol N 63,65 %, O 36,35 %, |
| Moment dipolaire | 0,160 83 D[3] |
| Propriétés physiques | |
| T° fusion | −90,8 °C[2] |
| T° ébullition | −88,5 °C[2] Décomposition à 300 °C |
| Solubilité | 1,5 g l−1 (eau, 15 °C)[2]. Soluble aussi dans l'acide sulfurique, l'éthanol, l'éther, les huiles. |
| Masse volumique | 1,23 g cm−3 (liquide, −89 °C)[2] 0,001 80 g cm−3 (gaz, 25 °C)[5] |
| Pression de vapeur saturante | 51,7 bar à 21 °C
|
| Point critique | 72,7 bar, 36,55 °C[7] |
| Vitesse du son | 263 m s−1 (0 °C, 1 atm)[8] |
| Thermochimie | |
| S0gaz, 1 bar | 219,96 J mol−1 K−1 |
| ΔfH0gaz | 82,05 kJ mol−1 |
| ΔvapH° | 16,53 kJ mol−1 (1 atm, −88,48 °C)[9] |
| Cp | |
| PCS | 82,1 kJ mol−1 (25 °C, gaz)[10] |
| Propriétés électroniques | |
| 1re énergie d'ionisation | 12,886 eV (gaz)[11] |
| Précautions | |
| SGH[12] | |
| H270, H280, H335, P370, P376 et P403 |
|
| SIMDUT[13] | |
   A, C, D2A, |
|
| NFPA 704 | |
| Transport[12] | |
| Inhalation | Asphyxiant si inhalé pur |
| Peau | Toxique si cryogénique ou compressé |
| Yeux | Toxique si cryogénique ou compressé |
| Données pharmacocinétiques | |
| CAM | 105 %vol[réf. souhaitée] |
| Métabolisme | Nul |
| Considérations thérapeutiques | |
| Classe thérapeutique | Anesthésique général, analgésique |
| Voie d’administration | Inhalatoire |
| Caractère psychotrope | |
| Catégorie | Hallucinogène dissociatif |
| Mode de consommation |
Inhalatoire |
| Autres dénominations |
Gaz hilarant |
| Risque de dépendance | Élevé[réf. nécessaire] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le protoxyde d'azote, ou monoxyde de diazote, oxyde nitreux, hémioxyde d'azote ou gaz hilarant, est un composé chimique de formule N2O. Ce gaz incolore a une odeur et un goût légèrement sucré. Il est utilisé en anesthésie, en chirurgie, en odontologie, en pédiatrie comme adjuvant (en mélange équimolaire avec du dioxygène) pour ses propriétés anesthésiques et antalgiques. Il est dit « gaz hilarant » car euphorisant à l'inhalation, d'où son usage comme drogue récréative hallucinogène[14],[15]. Comme comburant, il accroît la puissance des moteurs en compétition automobile. Avec l'acétylène H-C≡C-H, il est utilisé dans certains appareils d'analyse (spectrométrie d'absorption atomique[16]).
Ses émissions sont d'origine naturelle (forêts, océans) et humaine (agriculture, industrie chimique, principalement ; plus de 20 % d'augmentation dans l'air depuis l'époque pré-industrielle). Présent à l'état de traces dans l'air sec (330 parties par milliard[5]), c'est un gaz à effet de serre 273 fois plus puissant que le CO2. Il est également devenu le premier contributeur à la destruction de la couche d'ozone[17]. Des études scientifiques publiées en 2021 concluent que son coût social a été sous-estimé, car ne tenant pas compte de l'appauvrissement de la couche d'ozone stratosphérique, effet qui à lui seul pourrait augmenter de 20 % son impact négatif pour la santé humaine. Selon la même étude, ses liens avec d'autres effets de la pollution azotée pourraient rendre son « atténuation encore plus impérieuse » dans l'atmosphère[18]. Les engrais azotés, sont responsables d'une grande partie de l'augmentation des émissions de N2O ces dernières années. Sa concentration dans l'atmosphère croît depuis 150 ans (+ 2 % par décennie au rythme des années 2010), ce qui est préoccupant, car — comme le dioxyde de carbone — c'est un gaz à effet de serre persistant, à haut pouvoir réchauffant, qui s’accumule dans l'atmosphère où il contribue au dérèglement climatique. Au début des années 2020, la croissance récente des émissions de N2O dépasse certains des scénarios d'émission les plus pessimistes. Ce gaz est sous-estimé dans les inventaires nationaux qui ne tiennent pas compte de certaines sources naturelles et des limites méthodologiques d'attribution des sources anthropiques.
- ↑ Marc Gozlan, « Le protoxyde d'azote, un gaz hilarant qui ne fait pas du tout rire les médecins », Réalités biomédicales, 28 décembre 2018, Le Monde (consulté le 8 juillet 2019).
- OXYDE NITREUX, Fiches internationales de sécurité chimique .
- ↑ (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press/Taylor & Francis, , 89e éd., 2736 p. (ISBN 9781420066791, présentation en ligne), p. 9-50.
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Fiche renseignement, Gas Encyclopedia, Air liquide.
- (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, USA, McGraw-Hill, , 7e éd., 2400 p. (ISBN 0-07-049841-5), p. 2-50.
- ↑ (en) « Properties of Various Gases », sur flexwareinc.com (consulté le ).
- ↑ (en) William M. Haynes, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press/Taylor & Francis, , 91e éd., 2610 p. (ISBN 9781439820773, présentation en ligne), p. 14-40.
- ↑ (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press/Taylor & Francis, , 90e éd., 2804 p. (ISBN 9781420090840, présentation en ligne).
- ↑ (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press, , 83e éd., 2664 p. (ISBN 0849304830, présentation en ligne), p. 5-89.
- ↑ (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press/Taylor & Francis, , 89e éd., 2736 p. (ISBN 9781420066791, présentation en ligne), p. 10-205.
- Entrée « Nitrous oxide » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais) (JavaScript nécessaire).
- ↑ « Oxyde nitreux » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009.
- ↑ Clément Gérome, Agnès Cadet-Taïrou, Michel Gandilhon, Maitena Milhet, Magali Martinez et Thomas Néfau, « Substances psychoactives, usagers et marchés : les tendances récentes (2017-2018) », Tendances, OFDT, Observatoire français des drogues et des toxicomanies, no 129, (lire en ligne).
- ↑ Lose S, CedrAgir/Trend, Tendances récentes et nouvelles drogues, décembre 2018 (OFDT, Observatoire français des drogues et des toxicomanies).
- ↑ Futura, « Définition | Spectrométrie d'absorption – SAA | Futura Sciences », sur Futura (consulté le ).
- ↑ Erreur de référence : Balise
<ref>incorrecte : aucun texte n’a été fourni pour les références nomméesRandeniya2002 - ↑ (en) David R. Kanter, Claudia Wagner-Riddle, Peter M. Groffman et Eric A. Davidson, « Improving the social cost of nitrous oxide », Nature Climate Change, vol. 11, no 12, , p. 1008–1010 (ISSN 1758-678X et 1758-6798, DOI 10.1038/s41558-021-01226-z, lire en ligne, consulté le ).














