
Back هقزامتیلفوسفورآمید AZB Hexamethylfosforamid Czech Hexamethylphosphorsäuretriamid German Hexamethylphosphoramide English Hexametilfosforamida Spanish هگزامتیلفسفرآمید Persian Heksametyylifosforiamidi Finnish Hexaméthylphosphoramide French Heksametilfosforamida ID ヘキサメチルリン酸トリアミド Japanese
| Esametilfosforammide | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| esametilfosforammide | |
| Abbreviazioni | |
| HMPA | |
| Nomi alternativi | |
| triammide esametilfosforica esametilfosfammide ossido di tris(dimetilammino)fosfina | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C6H18N3OP |
| Massa molecolare (u) | 179,20 |
| Aspetto | liquido incolore |
| Numero CAS | |
| Numero EINECS | 211-653-8 |
| PubChem | 12679 |
| SMILES | CN(C)P(=O)(N(C)C)N(C)C |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,024 |
| Indice di rifrazione | 1,45792 (20 °C) |
| Solubilità in acqua | completamente miscibile |
| Coefficiente di ripartizione 1-ottanolo/acqua | 0,28 |
| Temperatura di fusione | 7,2 °C (280,35 K) |
| Temperatura di ebollizione | 233 °C (506,15 K) |
| Tensione di vapore (Pa) a 298,15 K | 9 |
| Proprietà tossicologiche | |
| DL50 (mg/kg) | 2.650 (orale, ratto) |
| Indicazioni di sicurezza | |
| Punto di fiamma | 105 °C (378,15 K) |
| Temperatura di autoignizione | 230 °C (503,15 K) |
| Simboli di rischio chimico | |

| |
| pericolo | |
| Frasi H | 350 - 340 [1] |
| Consigli P | 201 - 308+313 [2] |
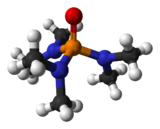
L'esametilfosforammide, spesso indicata con la sigla HMPA (derivante dall'inglese Hexamethylphosphoramide), è la triammide dell'acido fosforico dove tutti gli atomi di idrogeno sono sostituiti da gruppi metilici. La sua formula semistrutturale è quindi [(CH3)2N]3P=O o (Me2N)3P=O. A temperatura ambiente si presenta come un liquido incolore altobollente, fortemente igroscopico e solubile in acqua in ogni proporzione. È sospettata di essere carcinogenica e mutagenica.[3][4] Per tali motivi, pur essendo un ottimo solvente polare aprotico viene solo a volte impiegata come come tale o come reattivo nella sintesi organica.[5]
- ^ Scheda IFA-GESTIS, su gestis-en.itrust.de. URL consultato il 16 ottobre 2014 (archiviato dall'url originale l'11 novembre 2016).
- ^ Sigma Aldrich; rev. del 18.12.2014
- ^ (EN) PubChem, Hexamethylphosphoramide, su pubchem.ncbi.nlm.nih.gov. URL consultato il 12 maggio 2024.
- ^ (EN) Chi -Chu Lo e Pei -Min Chao, Replacement of carcinogenic solvent HMPA by DMI in insect sex pheromone synthesis, in Journal of Chemical Ecology, vol. 16, n. 12, 1º dicembre 1990, pp. 3245–3253, DOI:10.1007/BF00982095. URL consultato il 12 maggio 2024.
- ^ (EN) Robert R. Dykstra, Hexamethylphosphoric Triamide, John Wiley & Sons, Ltd, 15 aprile 2001, DOI:10.1002/047084289x.rh020, ISBN 978-0-471-93623-7. URL consultato il 12 maggio 2024.