| Egenschoppen in’n Vergliek | ||
| Naam | n-Butan[1] | Isobutan[2] |
| Strukturformel | 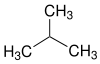
| |
| CAS-Tall | 106-97-8 | 75-28-5 |
| Summenformel | C4H10 | |
| Molare Masse | 58,12 g·mol−1 | |
| Kortbeschrieven | bi 20 °C un 1013 mbar gasförmig | |
| Smöltpunkt | −138,29 °C | −159,42 °C |
| Kaakpunkt | −0,50 °C | −11,7 °C |
| Dampdruck (20 °C) | 208 kPa | 301,9 kPa |
| Dicht bi 0 °C, 1013 hPa | 2,71 kg·m−3 | 2,70 kg·m−3 |
| Löslichkeit | 61 mg·l−1 | 49 mg·l−1 |
| Ünnere Explosionsgrenz (UEG) |
1,4 Vol% | 1,5 Vol% |
| 33 g·m−3 | 37 g·m−3 | |
| Bövere Explosionsgrenz (OEG) |
9,4 Vol% | 9,4 Vol% |
| 231 g·m−3 | 231 g·m−3 | |
De Butanen sünd en Stoffgrupp binnen de Grupp vun de Alkanen, de dör de Summenformel C4H10 kenntekent sünd. De Grupp besteiht blots ut twee Vertreders, de as n-Butan un iso-Butan betekent warrt un to’nanner isomer sünd. Bi beide Stoffen hannelt sik dat üm brennbore Gasen ahn Klöör, de licht fletig to maken gaht (Fletiggas). Se löst sik kuum in Water, dorför aver goot in Ethanol un Ether[3].
- ↑ Indrag to n-Butan in de GESTIS-Datenbank, afropen an’n 21. Februar 2013
- ↑ Indrag to Iso-Butan in de GESTIS-Datenbank, afropen an’n 21. Februar 2013
- ↑ Wissenschaft-Online-Lexika: Indrag to „Butanen“ in’t Lexikon der Chemie, afropen an’n 17. November 2011.
