
Back سيستين Arabic سیستین AZB Цыстын Byelorussian Цистин Bulgarian Cistin BS Cistina Catalan Cystin German Κυστίνη Greek Cystine English Cistino Esperanto
| Cistin | |||
|---|---|---|---|
 |
 | ||
| Identifikacija | |||
| CAS registarski broj | 56-89-3 | ||
| ChemSpider[1] | 575 | ||
| UNII | 48TCX9A1VT | ||
| KEGG[2] | |||
| ChEMBL[3] | CHEMBL366563 | ||
| Jmol-3D slike | Slika 1 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | C6H12N2O4S2 | ||
| Molarna masa | 240.3 g mol−1 | ||
| Opasnost | |||
| Podaci o bezbednosti prilikom rukovanja (MSDS) | External MSDS | ||
|
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |||
| Infobox references | |||
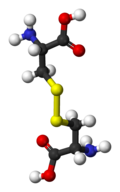
Cistin je dimerna aminokiselina formirana oksidacijom dva ostatka cisteina koja su kovalentno vezana disulfidnom vezom. Ovo organosumporno jedinjenje ima formulu (SCH2CH(NH2)CO2H)2. Cistin je beli prah, koji se topi na 247-249 °C. Otkrio ga je 1810 Vilijam Hid Volaston. Tek je 1899. bilo pokazano da se cistin može dobiti iz proteina. Te godine je bio izolovan iz goveđih rogova.[4] Putem formiranja disulfidnih veza unutar i između molekula proteina, cistin je značajan determinant tercijarne strukture većine proteina. Na primer, disulfidno vezivanje, zajedno sa vodoničnim vezama i hidrofobnim interakcijama, je parcijalno odgovorno za formiranje glutenske osnove hleba. Ljudska kosa sadrži aproksimativno 5% cistina po masi.[5]
- ↑ Hettne KM, Williams AJ, van Mulligen EM, Kleinjans J, Tkachenko V, Kors JA. (2010). „Automatic vs. manual curation of a multi-source chemical dictionary: the impact on text mining”. J Cheminform 2 (1): 3. DOI:10.1186/1758-2946-2-3. PMID 20331846.
- ↑ Joanne Wixon, Douglas Kell (2000). „Website Review: The Kyoto Encyclopedia of Genes and Genomes — KEGG”. Yeast 17 (1): 48–55. DOI:10.1002/(SICI)1097-0061(200004)17:1<48::AID-YEA2>3.0.CO;2-H.
- ↑ Gaulton A, Bellis LJ, Bento AP, Chambers J, Davies M, Hersey A, Light Y, McGlinchey S, Michalovich D, Al-Lazikani B, Overington JP. (2012). „ChEMBL: a large-scale bioactivity database for drug discovery”. Nucleic Acids Res 40 (Database issue): D1100-7. DOI:10.1093/nar/gkr777. PMID 21948594.
- ↑ „Cystine”. Encyclopædia Britannica. 2007.
- ↑ Gortner, R. A.; W. F. Hoffman, W. F. (1941), „l-Cystine”, Organic Syntheses; Coll. Vol. 1: 194