
Back بروميد الهيدروجين Arabic هیدروژن برومید AZB Бромавадарод Byelorussian Бромавадарод BE-X-OLD Бромоводород Bulgarian Bromovodík Czech Hydrogenbromid Danish Bromwasserstoff German Υδροβρώμιο Greek Hydrogen bromide English
| |||
| |||
| Imena | |||
|---|---|---|---|
| Priporočeno IUPAC ime
Hydrogen bromide[navedi vir] Opozorilo predogleda: Stran, ki uporablja Predloga:Navedi vir z nepodprtim parametrom »date« | |||
| Sistematično ime
Bromane[1] | |||
| Identifikatorji | |||
3D model (JSmol)
|
|||
| 3587158 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.030.090 | ||
| EC število |
| ||
| KEGG | |||
| MeSH | Hydrobromic+Acid | ||
PubChem CID
|
|||
| RTECS število |
| ||
| UNII | |||
| UN število | 1048 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Struktura | |||
| Oblika molekule | Linearna | ||
| Dipolni moment | 820 mD | ||
| Termokemija | |||
| Specifična toplota, C | 350,7 mJ/(K·g) | ||
| Standardna molarna entropija S |
198.696–198.704 J/(K·mol)[2] | ||
Std tvorbena
entalpija (ΔfH⦵298) |
−36,45...−36,13 kJ/mol[2] | ||
| Nevarnosti | |||
| Varnostni list | hazard.com | ||
| GHS piktogrami |  
| ||
| Opozorilna beseda | Pozor | ||
| H314, H335 | |||
| P261, P280, P305+351+338, P310 | |||
| NFPA 704 (diamant ognja) | |||
| Smrtni odmerek ali koncentracija (LD, LC): | |||
LC50 (srednja koncentracija)
|
2858 ppm (podgana, 1 h) 814 ppm (miš, 1 h)[4] | ||
| NIOSH (ZDA varnostne meje): | |||
PEL (Dopustno)
|
TWA 3 ppm (10 mg/m3)[3] | ||
REL (Priporočeno)
|
TWA 3 ppm (10 mg/m3)[3] | ||
IDLH (Takojšnja nevarnost)
|
30 ppm[3] | ||
Če ni navedeno drugače, podatki veljajo za material v standardnem stanju pri 25 °C, 100 kPa). | |||
| Sklici infopolja | |||
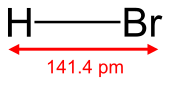
Vodikov bromid (tudi Bromvodik; HBr) je zelo jedka snov, ki je lahko v plinastem ali tekočem stanju. Spojine broma se uporabljajo v kemijski, fotografski in farmacevtski industriji. Vodikov bromid je brezbarven plin. Na vlažnem zraku se kadi. Vodna raztopina je podobna klorovodikovi kislini, soli so bromidi. Vodikov bromid ne gori. Pri segrevanju zaradi požara v okolici hladimo posode z razpršenim vodnim curkom. Vodikov bromid je diatomična molekula HBr. HBr je plin v standardnih pogojih. HBr kislina nastaja ob raztapljanju HBr v vodi. Obratno HBr lahko osvobodimo iz HBr hidrobromičnih kislinskih raztopin z dodatkom dehidracijskega sredstva, ampak ne z destilacijo. Vodikov bromid in hidrobromična kislina tako nista enaka ampak sta povezana. Kemiki pogosto naslavljajo hidrobromično kislino kot “HBr” v tej uporabi, medtem, ko je to razumljivo večini kemikov, to ni točno in lahko privede do zmešnjave pri ne specializiranih osebah. Na sobni temperaturi je HBr nevnetljiv plin z ostrim vonjem, v vlažnem zraku je kadeč zaradi nastajanja hidrobromične kisline. HBr je dobro vodotopen, nastaja hidrobromična kislinska raztopina katera je po težini 60,85% nasičena z HBr na sobni temperaturi. Vodne raztopine so po težini 47,6% HBr in nastaja mešanica obratni azeotrop v stanju stalnega vretja, ki vre na temperaturi 124,3 stopin celzij. Vrenje manj koncetriranih raztopin spušča H2O, dokler ni dosežena mešanica komponent, katera stalno vre.
- ↑ »Hydrobromic Acid - Compound Summary«. PubChem Compound. USA: National Center for Biotechnology Information. 16. september 2004. Identification and Related Records. Pridobljeno 10. novembra 2011.
- ↑ 2,0 2,1 Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. ISBN 978-0-618-94690-7.
- ↑ 3,0 3,1 3,2 NIOSH Pocket Guide to Chemical Hazards. »#0331«. National Institute for Occupational Safety and Health (NIOSH).
- ↑ »Hydrogen bromide«. Immediately Dangerous to Life and Health Concentrations (IDLH). National Institute for Occupational Safety and Health (NIOSH).


