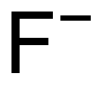Back Fluoried Afrikaans فلوريد Arabic فلورید AZB ফ্লোরাইড Bengali/Bangla Fluorur Catalan Fluoridy Czech Fluoride German ފްލޮރައިޑް DV Fluoride English Fluoruro Spanish
| Fluoride | |||
|---|---|---|---|
| |||
| Danh pháp IUPAC | Fluoride[1] | ||
| Nhận dạng | |||
| Số CAS | |||
| PubChem | |||
| KEGG | |||
| MeSH | |||
| ChEBI | |||
| ChEMBL | |||
| Ảnh Jmol-3D | ảnh | ||
| SMILES | đầy đủ
| ||
| Tham chiếu Gmelin | 14905 | ||
| Thuộc tính | |||
| Công thức phân tử | F− | ||
| Điểm nóng chảy | |||
| Điểm sôi | |||
| Nhiệt hóa học | |||
| Enthalpy hình thành ΔfH | −333 kJ mol−1 | ||
| Entropy mol tiêu chuẩn S | 145.58 J/mol K (gaseous)[2] | ||
| Các hợp chất liên quan | |||
| Anion khác | |||
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |||
Fluoride /ˈflʊəraɪd/,[3] /ˈflɔːraɪd/ là một anion hóa vô cơ, đơn phân tử của fluor với công thức hóa học F−. Fluoride là anion đơn giản nhất của fluor. Muối và khoáng chất của nó là các hợp chất phản ứng hóa học và hóa chất công nghiệp quan trọng, chủ yếu được sử dụng trong sản xuất hydro fluoride cho các chất fluorocarbon. Về độ âm điện và kích cỡ, ion fluoride tương tự như ion hydroxide. Các ion fluoride có mặt trên Trái Đất trong một số khoáng chất, đặc biệt là fluorit, nhưng chỉ có với số lượng vi lượng trong nước. Fluoride có một vị đắng đặc biệt. Nó không tạo thành màu cho muối fluoride.
- ^ “Fluorides – PubChem Public Chemical Database”. The PubChem Project. USA: National Center for Biotechnology Information. Identification.
- ^ “Fluorine anion”. NIST. Truy cập ngày 4 tháng 7 năm 2012.
- ^ Wells, J.C. (2008). Longman pronunciation dictionary (ấn bản thứ 3). Harlow, England: Pearson Education Limited/Longman. tr. 313. ISBN 9781405881180.. According to this source, /ˈfluː.əraɪd/ is a possible pronunciation in British English.